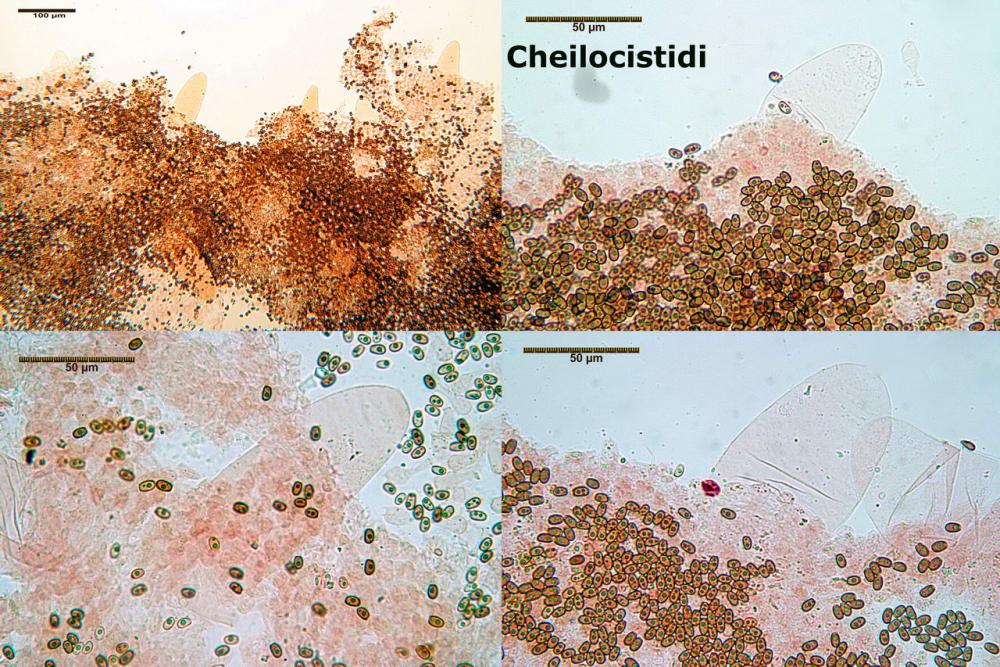
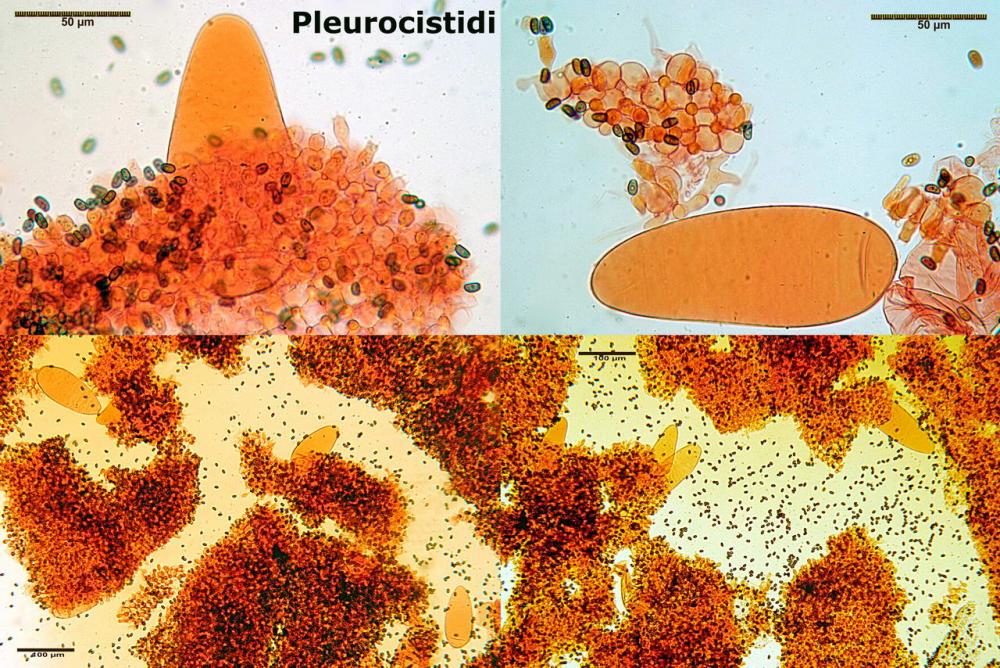
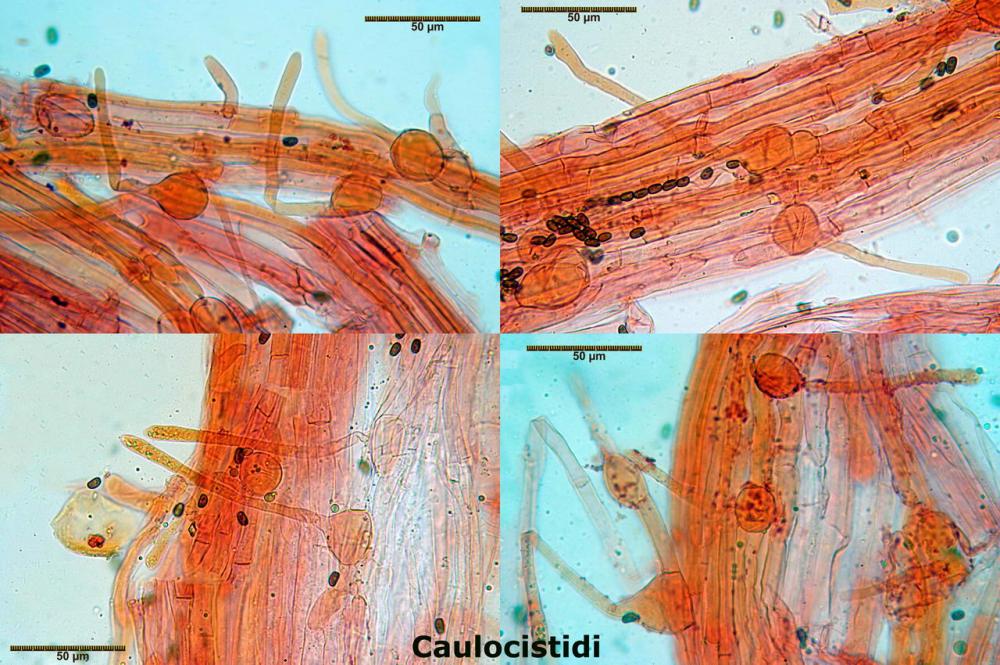
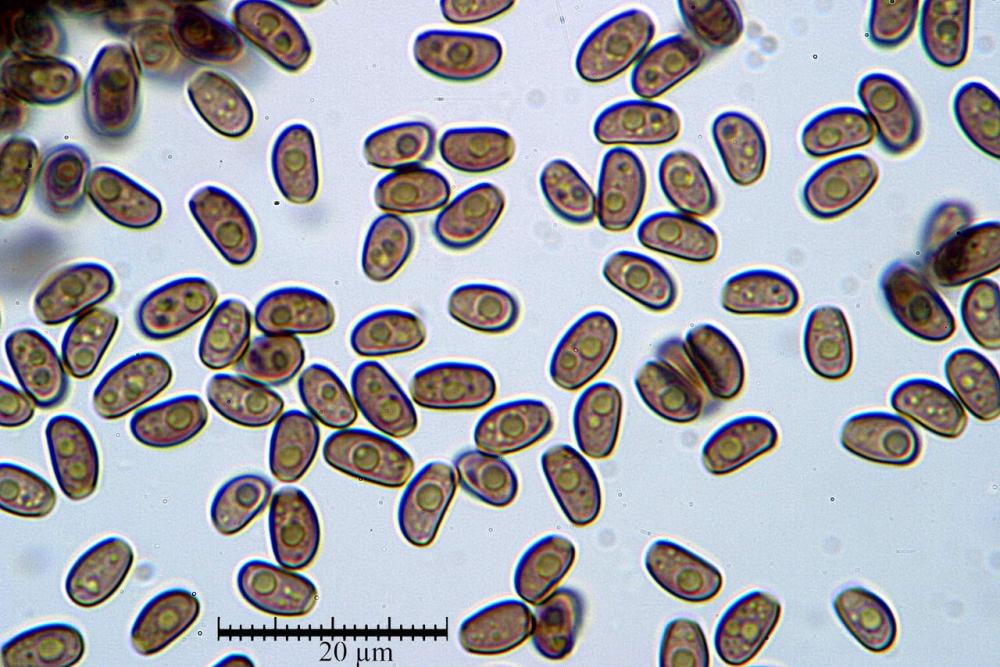
Habitat delle raccolte studiate nel secondo contributo
Le raccolte sono state effettuate in Località Laghetti di Noghere. Comune di Muggia (TS). Coordinate geografiche: 45°35'11.90"N 13°48'57.16"E. Altezza s.l.m.: 5.
Hebeloma ochroalbidum Bohus, (1972). N. scheda 2966. Data di ritrovamento 03/11/2005. Habitat: sette esemplari in diversi stadi di crescita, nei pressi del laghetto, sotto Populus nigra, Alnus glutinosa, in terreno argilloso. Legit: R., Cainelli, A. Aiardi. Det. M. Zugna, E. Bizio.
Coprinellus ellisii (P.D. Orton) Redhead, Vilgalys & Moncalvo: N. scheda 4014. Data di ritrovamento: 13/04/2009. Habitat: su piccolo tronchetto di Alnus glutinosa morto, a terra. Legit: Zugna Alberto, Zugna M. Det. Zugna M.
Lacrymaria lacrymabunda (Bull.) Pat., N. scheda: 2961. Data di ritrovamento: 03/11/2005. Habitat: Il ritrovamento è stato effettuato in zona umida con terreno argilloso, la specie vegetava su terra nuda e prato incolto, sotto Populus nigra, e Salix alba, in zona prativa ai bordi del laghetto. Legit: Zugna M. Det. Zugna M.
Materiali e Metodi
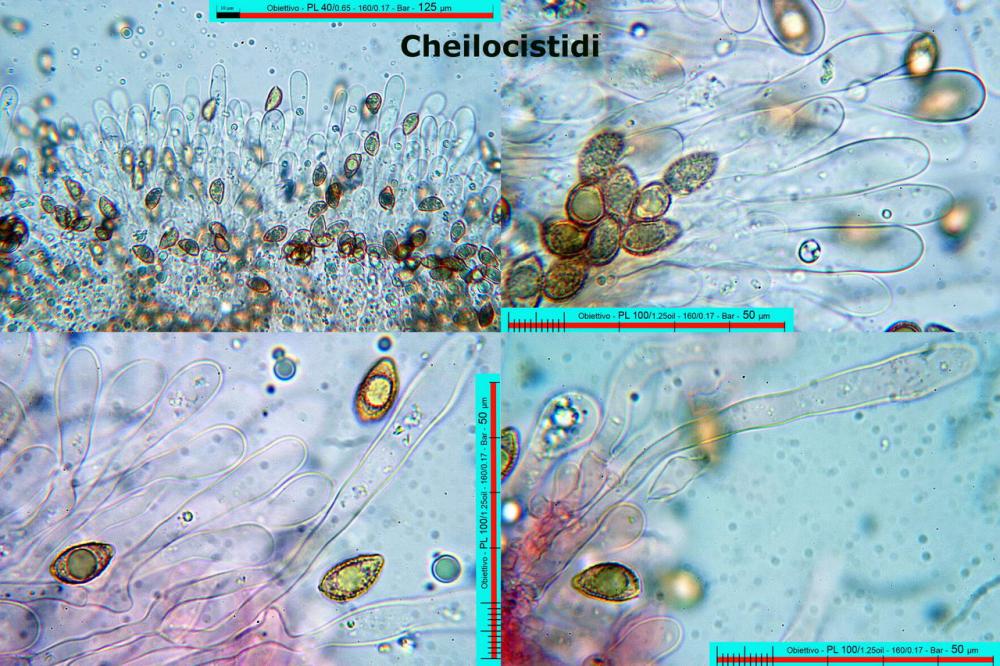
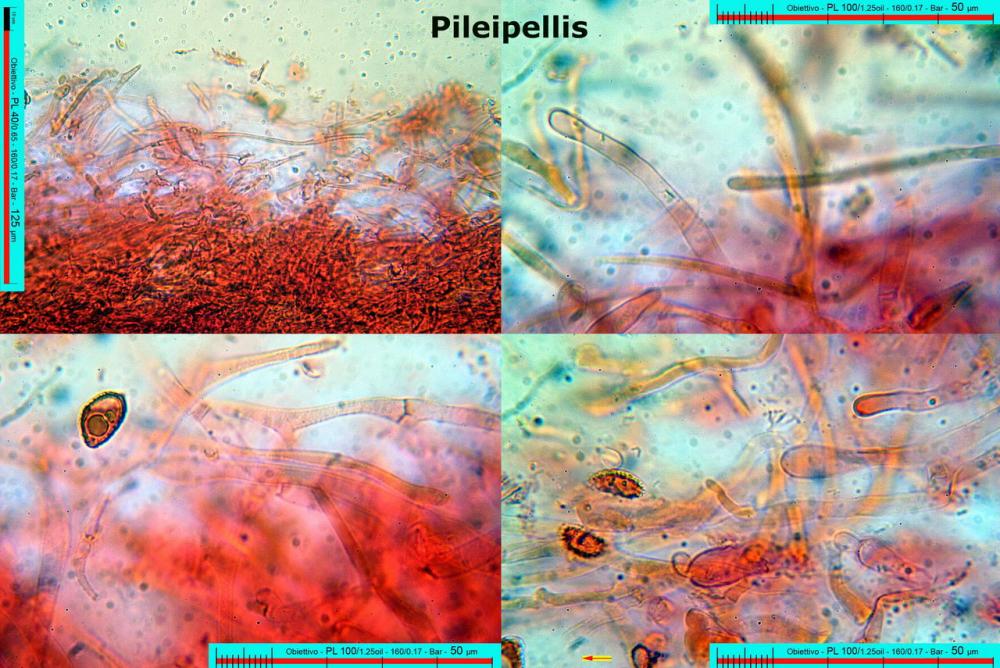
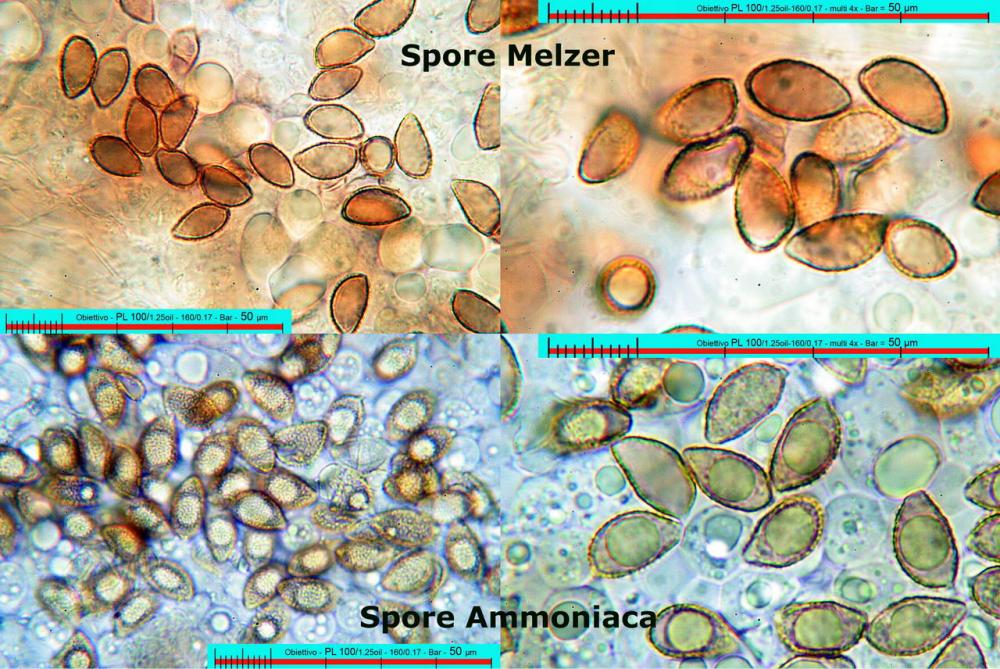
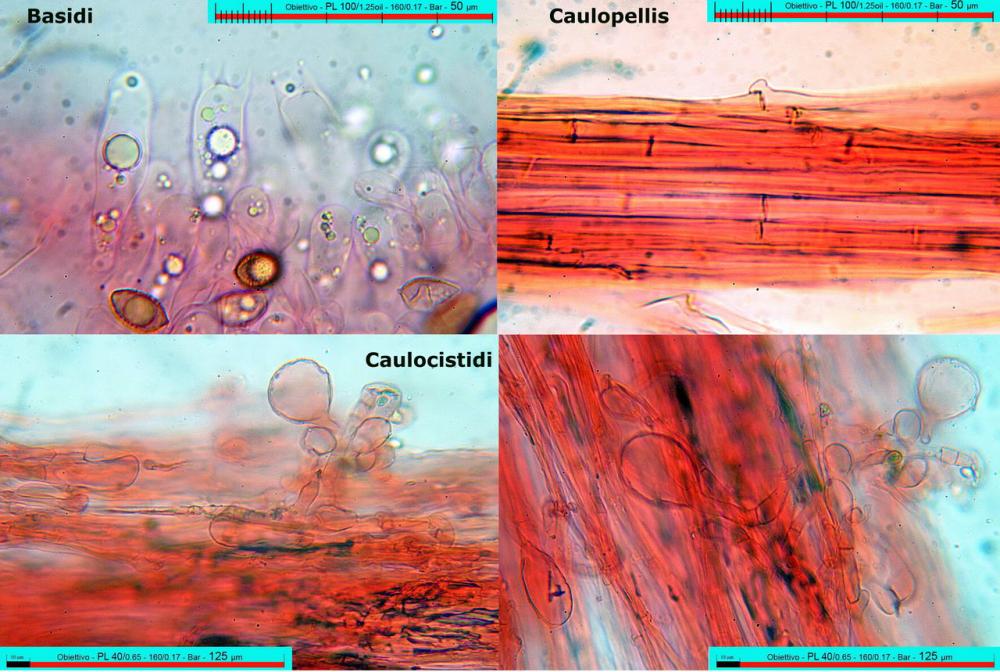
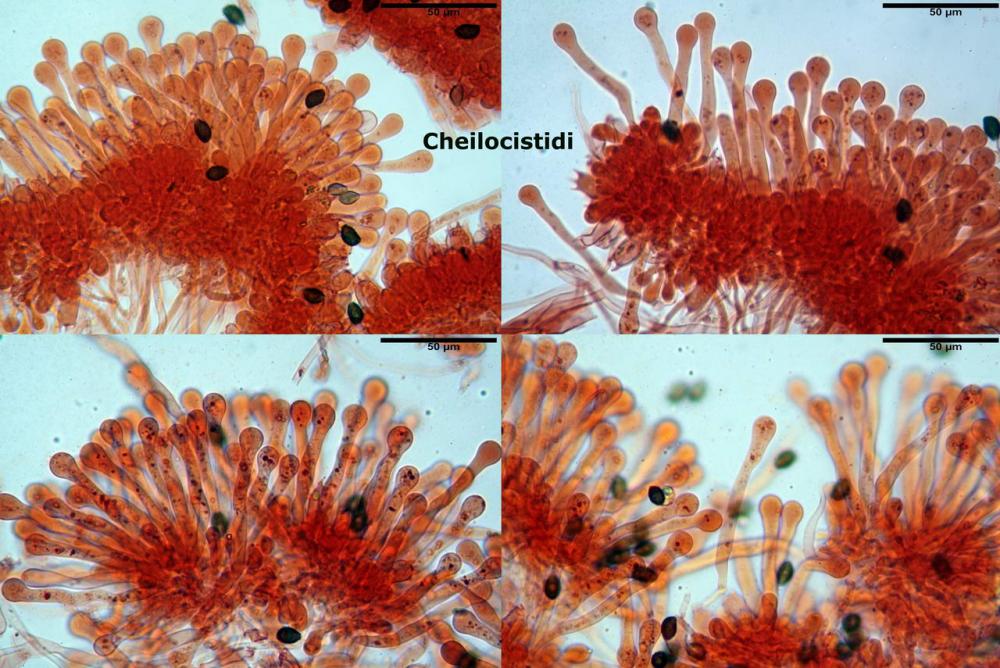
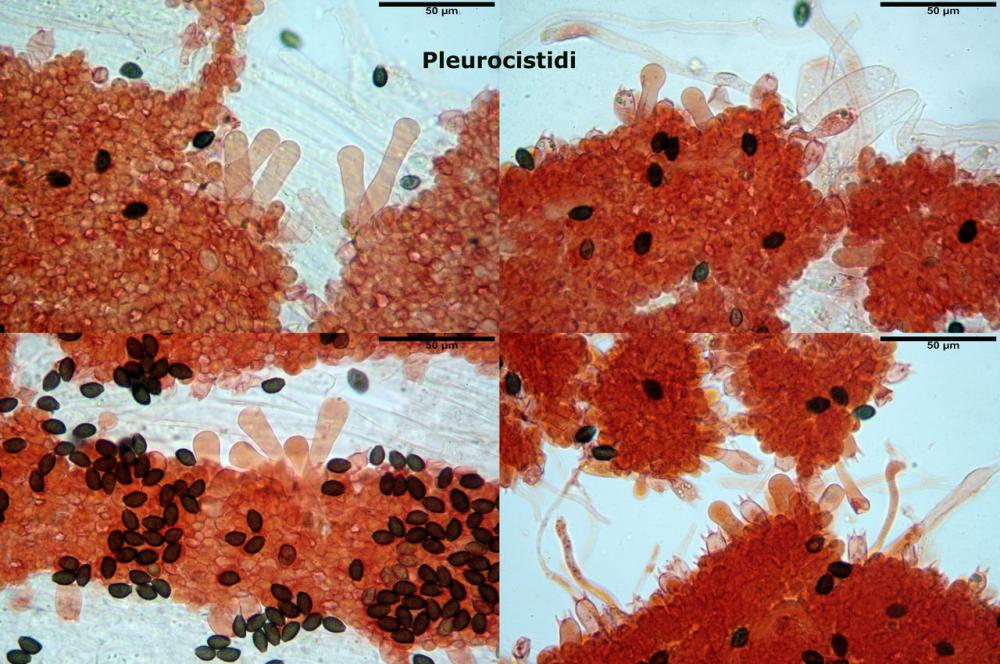
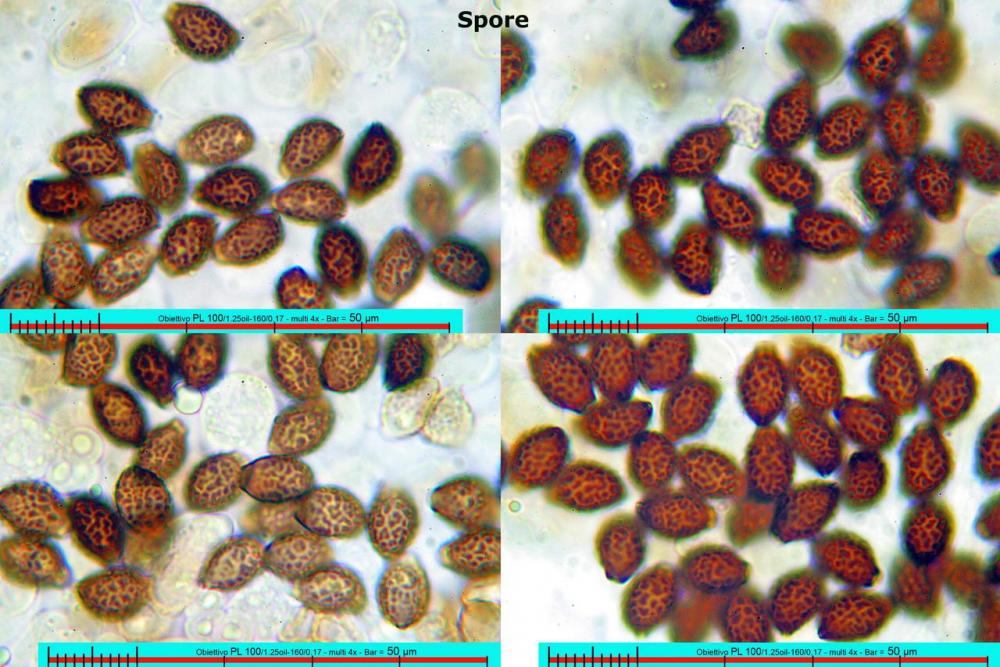
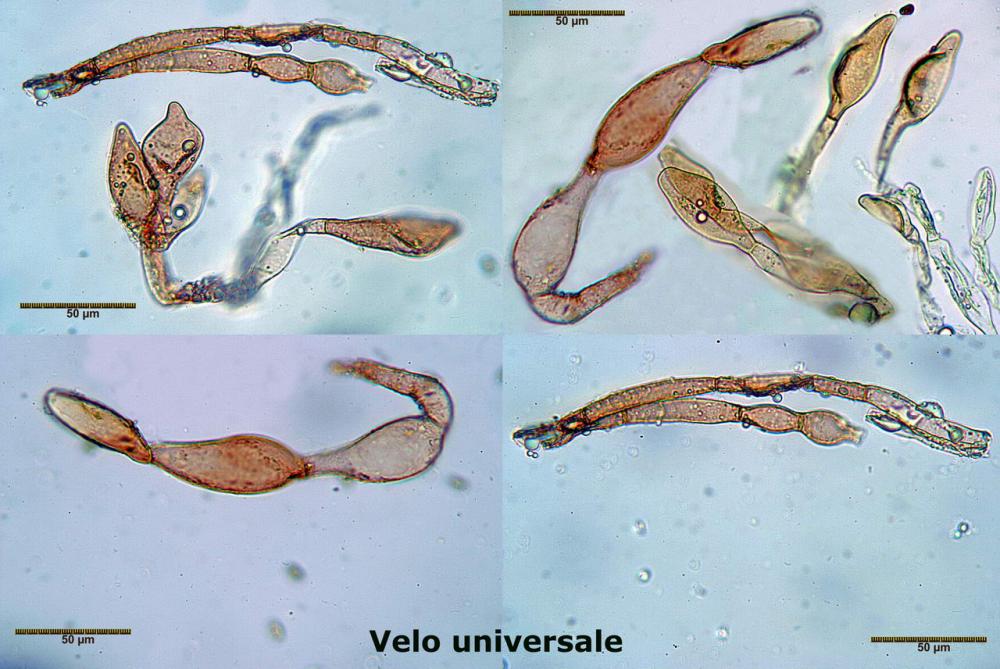
Lo studio microscopico è stato eseguito su materiale fresco. I preparati sono stati montati e osservati in H2O, ove necessario colorati con Rosso Congo Anionico per meglio evidenziare le differenti tipologie cellulari. Il reagente di Melzer è stato utilizzato per l’accertamento della destrinoidia delle spore. Le misure microscopiche sono state eseguite con il software di calcolo Mycométre gentilmente fornitoci dal Sig. Georges Fannechère e prelevabile all’indirizzo http://mycolim.free.fr. Le misure sporali si riferiscono a 100 unità, effettuate in proiezione laterale, ottenute da sporata o prelevate da altre zone non imeniali, scartando dal calcolo le spore ancora evidentemente immature e senza tener conto delle ornamentazioni che, nel caso, si sono misurate a parte. Per i rimanenti elementi cellulari, si sono eseguite un minimo di venti misure per tipologia.
Per la terminologia riguardante la tipologia delle caratteristiche macro e microscopiche, si fa riferimento a Else C. Vellinga 1998: (Flora Agaricina Neerlandica 1- Chapter 8; Glossary).
Per quanto riguarda la nomenclatura aggiornata e gli Autori delle specie, nella maggior parte dei casi, si è fatto riferimento a Index Fungorum http://www.indexfungorum.org/ e http://www.mycobank.org/MycoTaxo.aspx .
Le foto macro sono eseguite in habitat e/o, se necessario, in studio, con l’ausilio di una fotocamera Reflex Canon EOS D60 + obiettivo Canon EF 100mm f/2.8 Macro USM. Le foto concernenti la microscopia, sono state eseguite con l’ausilio della medesima fotocamera, posta sul terzo occhio del trinoculare di un microscopio biologico Optech Biostar B5, supportato da ottiche Plan-APO, illuminazione alogena 12V-50 W a luce riflessa con regolatore d'intensità.
Le collezioni sono depositate presso l'erbario A.M.B. Gruppo di Muggia e del Carso (E.G.M.C.), con i numeri riportati di seguito al binomio nel paragrafo dei dati delle raccolte.
Bibliografia
Bon M., 1992: Clé monographique des espèces galero-nauriocoides. Doc. Myc. Tome xxi, fasc. 84: 76.
Bon M., 2002: Clé de determination du genre Hebeloma. Documents mycologiques, tome XXXI, fascicule n°123, 3-40.
Breitenbach J. & F. Kränzlin, 1995: Champignons de Suisse, tome 5. Mykologia, lucerne.
Breitenbach J. & F. Kränzlin, 1995: Champignons de Suisse; tome 4. Lucerne.
C. Papetti, G. Consiglio, G. Simonini, 2001: Atlante fotografico dei funghi d'Italia - vol. 1.
Cetto, 1987: I funghi dal vero vol.5, pl.n.1747
Courtecuisse R. & B. Duhem, 1994: Guide des champignons den France et d’Europe. Delachaux et niestlé, p. 362
Gennari A., 2005: 501 funghi. Arezzo
Hausknecht A. & Krisai - Greilhuber I., 1997: Some rare agaricales with brown or darker spores. Fungi non delineati ii: 1-32. Libreria Mykoflora-Alassio.
index fungorum: http://www.indexfung...names/names.asp
Kühner R. & H. Romagnesi, 1974: flore analitique des champignons superieurs, paris.
Malençon G. & Bertault R., 1970: Flore des champignons supérieurs du Maroc. Tome i. Rabat
Moser M., 1986: Guida alla determinazione dei funghi, vol. 1, Trento.
Noordell. M.E., Kuyper Th. W. & E. C. Vellinga, 2005: Flora Agaricina Neerlandica, vol. 6
Noordeloos M.E., 1992: Fungi Europei n°5. Entoloma: 213-214, 726.
Noordeloos M.E., 1998: Flora Agaricina Neerlandica n° 1: 111.
Noordeloos M.E., 2004: Fungi Europei n° 5a. Entoloma, supplemento: 920-921.
Orton P.D., 1972: notes on British agarics : iv, notes from the royal botanie garden, Edinburgh 32-135-150
Orton P.D. & R. Walting, 1979: British Fungus Flora 2, Coprinacee part 1 : Coprinus, Edinburgh.
Roy Watling & Norma M. Gregory, 1987: British Fungus Flora. Vo1.5 Strophariaceae & Coprinaceae
Uljé' C. B. & M. E., Noordeloos, 1997: Studies in Coprinus iv. Persoonia 16: 265m, 3.
Vesterholt J., 2005: the genus Hebeloma; fungi of Northern Europe, vol. 3.
Zugna M. 2015: Il biotopo dei Laghetti delle Noghere. Primo contributo. Bollettino del Centro Micologico Friulano. 2015.



 Questa discussione è bloccata
Questa discussione è bloccata